Bambini, farmaci e pancreatite
La pancreatite in età pediatrica è un’entità quasi certamente sottostimata, che negli ultimi 20 anni ha mostrato un’incidenza crescente fino a raggiungere i 3-13/100.000 casi/anno.1,2 Anche la sua classificazione ha richiesto una messa a punto da parte del Gruppo di studio internazionale INSPPIRE che ha definito i criteri diagnostici clinico-strumentali delle pancreatiti acute, acute ricorrenti e croniche nel bambino3 Se nell’adulto l’eziologia biliare e il consumo di alcol sono i principali determinanti di rischio, in pediatria predominano i fattori genetici, anatomici, metabolici e tossici.4,5 Tra questi ultimi, i farmaci costituiscono la quota prevalente, contribuendo in oltre un quarto dei casi ed essendo associati ad altri fattori di rischio in almeno un terzo dei pazienti.6 Ne discende la difficoltà, talora, di definire con certezza la genesi farmacologica del danno pancreatico, fatto che, insieme alla relativa rarità dell’evento e alla modesta numerosità delle casistiche disponibili, rende impossibile stabilire la reale incidenza del fenomeno.
Trivedi et al.7 nel 2005 e Badalov et al.8 nel 2007 hanno proposto algoritmi diagnostici per consentire la migliore definizione del rapporto causa-effetto. I meccanismi del danno possono essere diversi: immuno-mediato o da ipersensibilità, tossico diretto, infiammatorio o da tossicità mitocondriale.9 Solo tre farmaci - paracetamolo, eritromicina e carbamazepina - sono stati associati a una pancreatite da sovradosaggio nel bambino, mentre la maggior parte delle reazioni sembra essere di natura idiosincrasica e quindi imprevedibile, non dose-dipendente e a bassa incidenza.
L’insorgenza dei sintomi è insidiosa con addominalgia e sintomi gastrointestinali aspecifici (nausea, vomito, febbre, tensione addominale; entro poche ore si assiste a una elevazione di amilasi e lipasi di oltre tre volte il limite di norma. Rimossa la causa farmacologica, le amilasi tendono a ridursi nell’arco di 48-72 ore mentre le lipasi possono rimanere alterate anche per 7-14 giorni.
I farmaci più coinvolti
I farmaci più spesso coinvolti sono gli antiepilettici (primo tra tutti l’acido valproico), l’asparaginasi, l’azatioprina, la mesalazina e i corticosteroidi, ma anche antibiotici, farmaci psichiatrici, i FANS, gli antilipemici, gli antipertensivi, gli ipoglicemizzanti e gli antivirali (vedi Tabella).4,10
Tabella 1. Farmaci responsabili di pancreatite secondo la classificazione di Badalov et al.8
| Classe Ia | Classe Ib | Classe II | Classe III | Classe IV |
|---|---|---|---|---|
| α-metildopa α-metildopa Acido valproico Azodisalicilato Bezafibrato Cannabis Carbimazolo Codeina Citosina Arabinoside Dapsone Enalapril Furosemide Isoniazide Mesalazina Metronidazolo Pentamidina Pravastatina Procainamide Piritonolo Simvastatina Stibogluconato Sulfametoxazolo Sulindac Tetraciclina | Acido trans-retinoico Amiodarone Azatioprina Clomifene Desametasone Ifosfamide Lamivudina Losartan Linestrenolo/metoxietinilestradiolo 6-mercaptopurina Meglumina Metimazolo Nelfinavir Noretindronato/mestranolo Omeprazolo Premarin Cotrimossazolo | Clorotiazide Clozapina Didanosina Eritromicina Estrogeni L-asparaginasi Paracetamolo Pegaspargasi Propofol Tamoxifene | Alendronato Atorvastatina Carbamazepina Captopril Ceftriaxone Clortalidone Cimetidina Claritromicina Ciclosporina Idroclorotiazide Indometacina Interferone/ribavirina Irbesartan Isotretinoina Ketorolac Lisinopril Metolazone Metformina Minociclina Mirtazapina Naproxene Paclitaxel Ponatinib Prednisone Prednisolone Sali d’oro | Acido etacrinico Acido mefenamico Ampicillina Bendroflumetiazide Benazepril Betametasone Capecitabina Cisplatino Colchicina Ciclofosfamide Ciproeptadina Danazolo Diazossido Diclofenac Difenoxilato Doxorubicina Famciclovir Finasteride 5-Fluorouracile Fluvastatina Gemfibrozil Interleuchina-2 Ketoprofene Lovastatina Nitrofurantoina Octreotide Ormoni adrenocorticoidi Oxifenbutazone Penicillina |
Spesso il farmaco è implicato come “concausa” in presenza di altri fattori di rischio, tipicamente quello genetico (è il caso delle tiopurine) o per altre patologie sottostanti (è il caso della malattia di Crohn). Su una casistica di 271 bambini con pancreatite, in 55 (25,6%) è stata individuata una causa farmacologica (10 accertata, 4 probabile e 2 possibile).6 Il 20% era affetto da epilessia, il 20% da leucemia, l’11% da malattia di Crohn e il 5% da colite ulcerosa. Gli steroidi erano i farmaci più spesso implicati, seguiti da acido valproico, mesalazina e cotrimossazolo. Nel 35% dei casi si trattava di un’associazione di due o più farmaci. Rispetto alle altre cause di pancreatite, i bambini con pancreatite associata a farmaci erano sottoposti più frequentemente a TC, avevano un ricovero più lungo e con maggiore impiego di nutrizione parenterale. In uno studio Cofini et al. riportano che il 13,5% dei casi di pancreatite (7/52) era attribuibile a farmaci, 4 dei quali in trattamento con acido valproico.11
La pancreatite da acido valproico non dipende dai livelli sierici del farmaco e può verificarsi in qualsiasi momento nel corso della terapia con un range che va da 2 a 84 mesi di trattamento.13,14 Il farmaco deve essere sospeso e sostituito per l’alto rischio di recidiva, anche complicata, della pancreatite.15 E’ stato riportato che bambini in monoterapia o politerapia antiepilettica (acido valproico, levetiracetam, carbamazepina, oxcarbamazepina, etosuccimide, lamotrigina, clonazepam) hanno livelli significativamente più alti di lipasi e amilasi rispetto ai controlli, pur in assenza di segni clinici di pancreatite. I livelli di enzimi pancreatici erano paragonabili tra chi era in mono e politerapia e tra chi utilizzava farmaci antiepilettici tradizionali o di seconda generazione.16 E’ pertanto verosimile che diversi farmaci antiepilettici (oltre all’acido valproico) abbiano potenzialità lesive sul pancreas e che il fenomeno sia sottostimato per una scarsa consuetudine, in ambito pediatrico, al dosaggio di lipasi e amilasi sieriche.
Nei pazienti con malattia infiammatoria cronica intestinale il rischio di pancreatite è 2,1 e 4,3 volte rispettivamente per la colite ulcerosa e per la malattia di Crohn. In questi pazienti, l’incidenza della pancreatite farmaco-indotta è pari al 15-63% e ne sono responsabili azatioprina, sulfasalazina e 5-ASA con una reazione di ipersensibilità dose e tempo non dipendente. E’ un effetto avverso solitamente di lieve entità e che si risolve da sé alla sospensione del trattamento. Un tentativo di reintroduzione del farmaco sospetto è possibile, a patto di monitorare attentamente l’andamento degli enzimi pancreatici sierici.17,18
Nell’ambito delle malattie infiammatorie croniche intestinali riveste particolare interesse l’azatioprina, farmaco ampiamente utilizzato anche in età pediatrica e responsabile di pancreatite nel 4-7% dei pazienti. Alcuni aplotipi HLA (DQA1*02:01 e DRB1*07:01) sembrano comportare un significativo fattore di rischio aggiuntivo (odds ratio 2,59) per sviluppare una pancreatite in corso di trattamento, con una frequenza pari al 9% negli eterozigoti e al 17% negli omozigoti.19,20
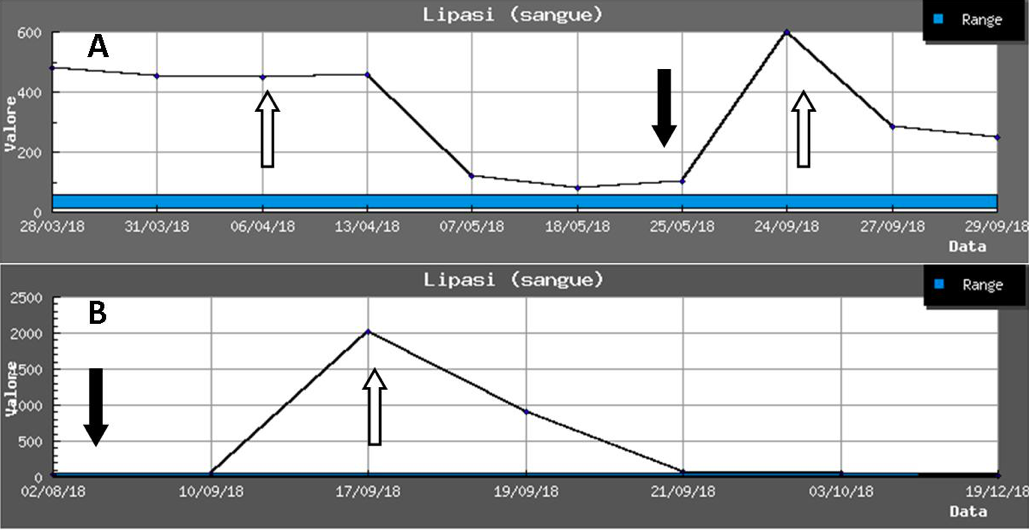
In conclusione, la pancreatite nel bambino è un evento certamente meno raro di quanto comunemente apprezzato e le reazioni avverse a farmaci ne rappresentano una quota non trascurabile. E’ necessario un indice di sospetto elevato e una buona conoscenza dei farmaci potenzialmente responsabili per interpretare correttamente la sintomatologia, spesso aspecifica e insidiosa. A titolo esemplificativo, riportiamo nella Figura, l’andamento delle lipasi in due adolescenti con pancreatite da clozapina (A) e da azatioprina (B).
Figura. Modificazione delle lipasi in due adolescenti in terapia con: A) clozapina, B) azatioprina [le frecce nere indicano l’introduzione, le frecce bianche la sospensione del farmaco]
- Gastroenterology 2019;156:1969-78. CDI
- Gastroenterology 2018;155:469-78.e1 CDI
- JPGN 2012;55:261-5 CDI
- JPGN 2016;62:609-17 CDI
- JAMA Pediatr 2016;170:562-9 CDI
- JPGN 2011:53:423-8 CDI
- J Clin Gastroenterol 2005;39:709-16 CDI
- Clin Gastroenterol Hepatol 2007;5:648-61 CDI
- P&T 2013;38:349-51 CDI
- Pancreas 2018;47:1328-36 CDI
- G Chir 2015;36:158-60 CDI
- PloS ONE 2014;9:e108970 CDI
- Pediatrics 2006;118:1660-3 CDI
- J Pediatr Pharmacol Ther 2020;25:256-60 CDI
- Cureus 2015;7:e297 CDI
- Child Neurol Open 2016;3:1-6.
- Pediatr Gastroenterol Hepatol Nutr 2012;15:272-5 CDI
- Pancreas 2019;48:488-95.
- Nat Genet 2014;46:1131-4 CDI
Enrico Valletta1, Michele Gangemi2
1 UO Pediatria, Ospedale G.B. Morgagni - L. Pierantoni, AUSL Romagna, Forlì
2 Pediatra, Verona